
中山大学吴桐/谭彩萍/程斌CEJ:内量网靶向的铱(III)光敏剂取PD-L1克制剂协同删效口腔鳞癌光免疫治疗
口腔鳞癌是头颈部常见的恶性肿瘤之一,低肿瘤免疫本性及免疫克制微环境是其常规治疗成效不佳的重要起因。连年来基于免疫检查点阻断的肿瘤免疫疗法深具潜力,但单一免疫疗法正在口腔鳞癌应答率有余20%。光动力疗法(PDT)可有效杀伤肿瘤细胞,并诱导肿瘤细胞发作免疫本性死亡(ICD)激活免疫反馈。如何真现PDT取免疫疗法的协同删效,是目前临床抗肿瘤免疫治疗面临的次要困境。 2023年8月,中山大学从属口腔病院吴桐(点击查察引见)、程斌教授(点击查察引见)团队结折中山大学化学学院谭彩萍教授(点击查察引见)团队正在Chemical Engineering Journal 纯志颁发钻研论文,将疏水性长链修饰配体取环金属化铱(III)光敏局部偶联,制备了一种新型内量网靶向的金属光敏剂Ir1。正在可见光(425 nm)照耀下,Ir1通过I/II型光动力门路诱导活性氧生成,激发内量网应激,并诱导肿瘤细胞ICD以加强免疫本性。同时,Ir1介导的PDT可促进PD-L1表达上调,为光动力-免疫协同治疗供给了根原。正在4NQO诱癌大鼠模型中,光动力-免疫结折治疗鲜亮遏行上皮恶性转化进程。正在移植瘤小鼠模型中,Ir1 介导的PDT诱导树突状细胞分化成熟激活抗本呈递,活化CD4+和CD8+T细胞分泌抗肿瘤细胞因子(TNF-α、IFN-γ),并结折PD-L1克制剂阻断免疫检查点重塑肿瘤免疫微环境,促进“冷肿瘤”向“热肿瘤”改动,真现口腔鳞癌光动力-免疫治疗协同删效。综上,Ir1不只能孕育发作较强的光动力效应,也能加强肿瘤免疫本性激活免疫反馈,同时结折PD-L1克制剂重塑部分免疫微环境,加强肿瘤杀伤做用。该钻研为金属光敏ICD诱导剂结折免疫检查点克制剂的口腔鳞癌光免疫治疗供给了一种新战略。
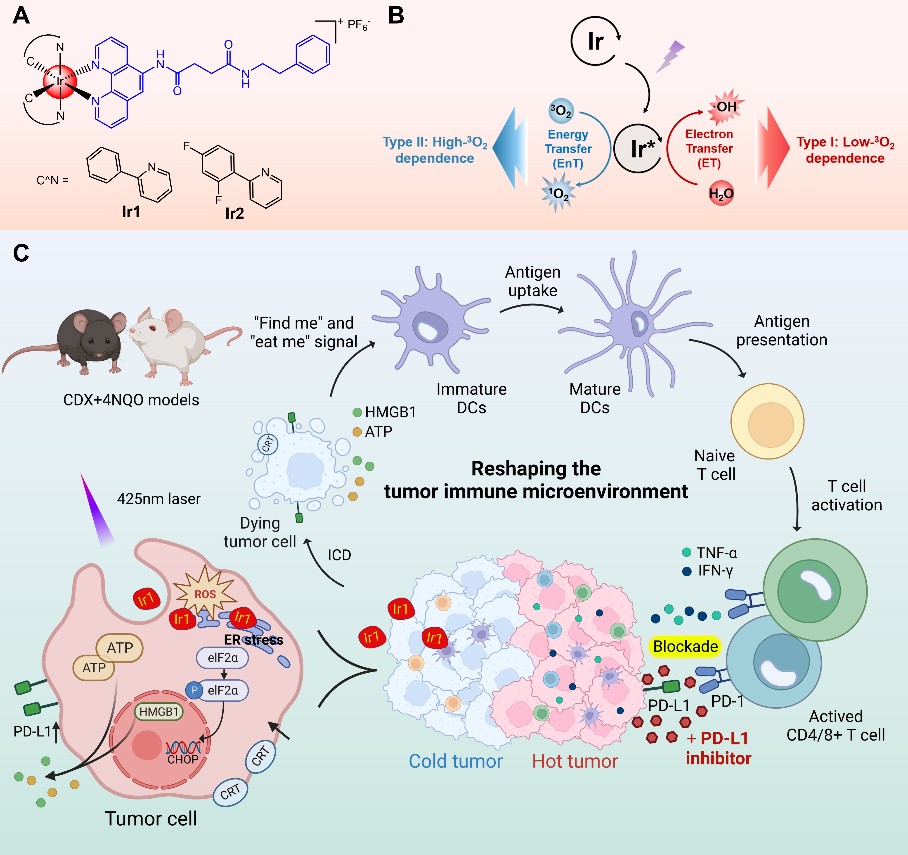
图1. Ir1分解及其取PD-L1克制剂协同介导口腔鳞癌光免疫治疗形式图
该项工做获得了广州市科技筹划名目(202206080009)和国家作做科学基金(22022707、22177142)撑持。吴桐主任医师、谭彩萍教授、程斌教授为原文的怪异通讯做者;周嘉颖(博士钻研生)、沈庆华(硕士钻研生)、洪晓婧(硕士钻研生)为原文的怪异第一做者。
本文(扫描或长按二维码,识别后曲达本文页面,或点此查察本文):

Synergization of an endoplasmic reticulum-targeted iridium(III) photosensitizer with PD-L1 inhibitor for oral squamous cell carcinoma immunotherapy
Jia-Ying Zhou#, Qing-Hua Shen#, Xiao-Jing Hong#, Wu-Ya Zhang, Qiao Su, Wu-Guo Li, Bin Cheng*, Cai-Ping Tan*, Tong Wu*
Chem. Eng. J., 2023, 474, 145516, DOI: 10.1016/j.cej.2023.145516
导师引见
吴桐
hts://ss.V-molss/uniZZZersity/faculty/347469
程斌
hts://ss.V-molss/uniZZZersity/faculty/347470
谭彩萍
hts://ss.V-molss/uniZZZersity/faculty/15392
假如篇首说明了授权起源,任何转载需与得起源方的许诺!假如篇首未出格说明缘故,原文版权属于 X-MOL ( V-molss ), 未经许诺,回绝转载!
点击分享
支藏
撤消支藏